ヘモフィール®
製品コンセプト
東レが有する「素材」技術によって開発された持続緩徐式血液濾過器ヘモフィール®は、独自に開発したポリメチルメタクリレート(PMMA)を膜素材とし、サイトカイン(IL-6)等の各種の病因物質の除去を行う「ヘモフィール®CH」、素材として広く使用されているポリスルホンを膜素材とし、透水性能の持続性を図る「ヘモフィール®SNV」の、それぞれ特性の異なる材質からなる2種類のフィルターがあります。
資料ダウンロード

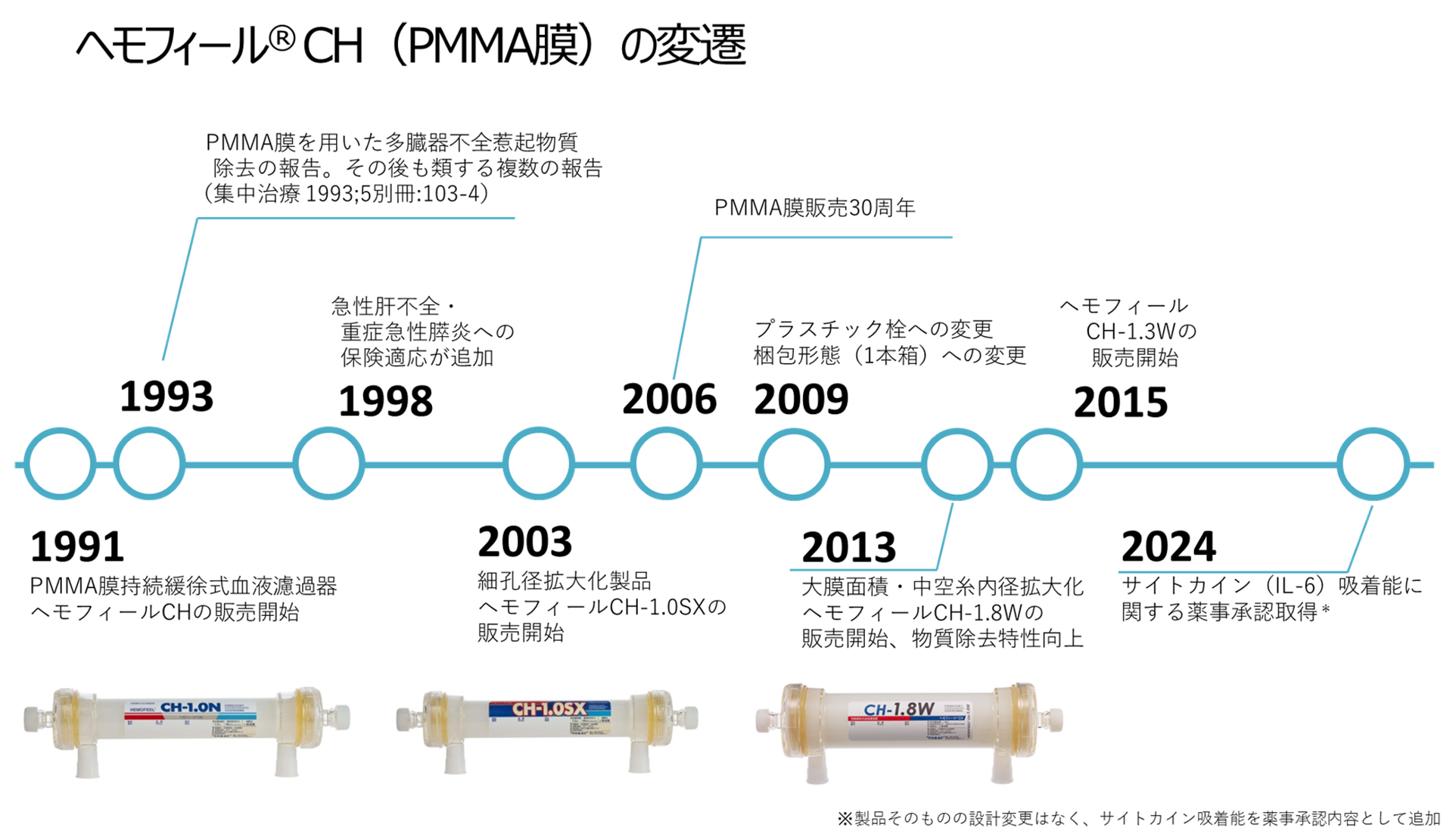
持続緩徐式血液濾過器 ヘモフィール®CH
東レ独自のPMMA膜技術による生体適合性と病因タンパク吸着の両立
-サイトカイン除去の新展開

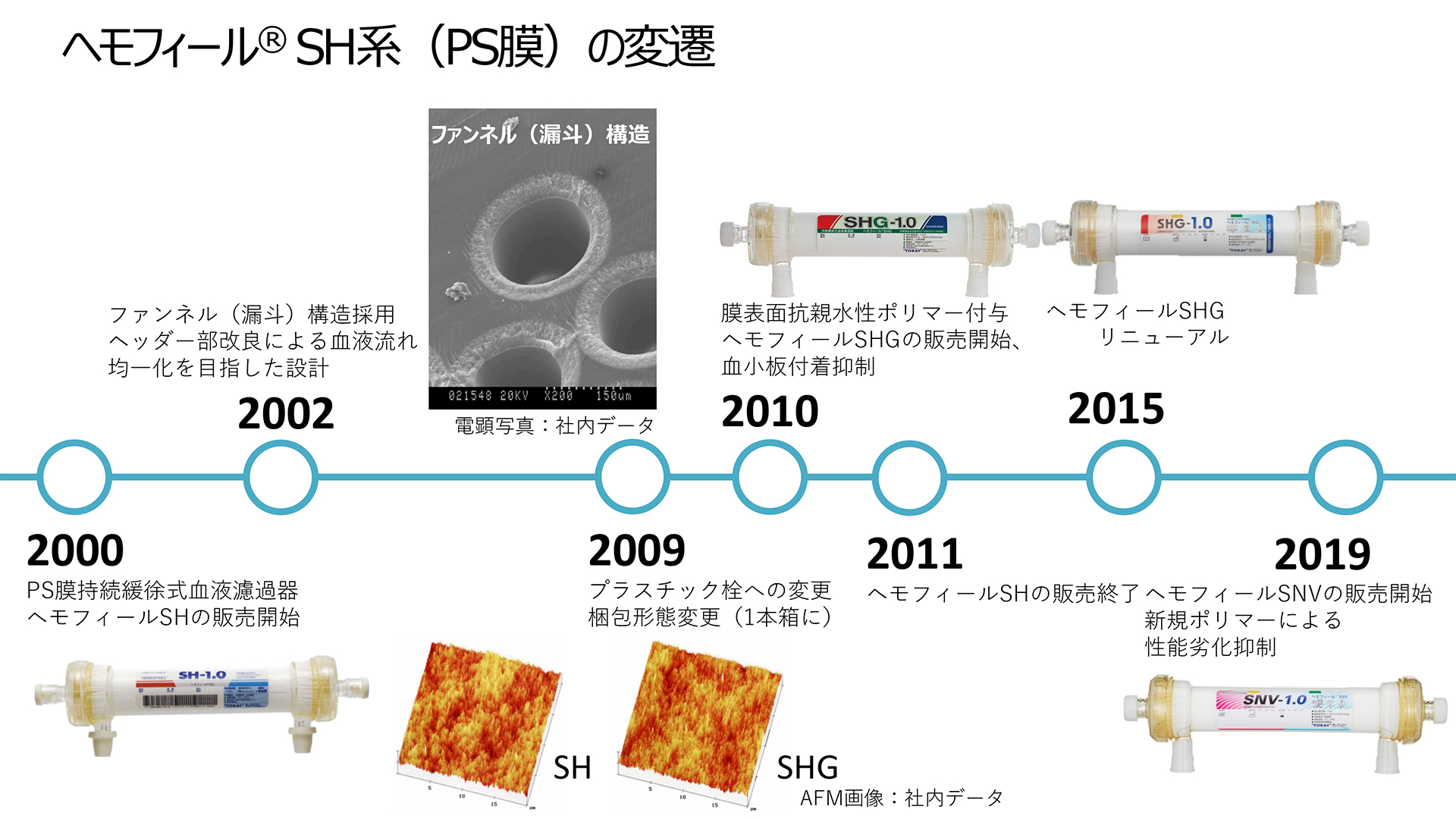
持続緩徐式血液濾過器 ヘモフィール®SNV
東レ独自のNVポリマー技術により性能劣化を防ぎ、持続性の向上を図りました。
開発の経緯
製品仕様
ヘモフィール®CH

| 販売名 | ヘモフィール®CH |
|---|---|
| 一般的名称 | 持続緩徐式血液濾過器 |
| 承認番号 | 20300BZZ00624000 |
| クラス分類 | 高度管理医療機器(クラスⅢ) |
| 特定保険医療材料 | 保険償還 II 040 人工腎臓用特定保険医療材料(回路を含む。) (4)持続緩徐式血液濾過器 ① 標準型 ア 一般用 CH-0.6W、CH-1.3W、CH-1.8W イ 超低体重患者用 CH-0.3W |
| 製造販売元 | 東レ株式会社 |
| 販売元 | 東レ・メディカル株式会社 |
型番・仕様等
- 性能はIn vitro値であり、臨床では使用条件の違いにより異なります。
- ご使用に際しては製品の注意事項等情報をご参照下さい。
- QB=100±4mL/min、37±1℃、TMP=6.7kPa(50mmHg)、37±1℃、Ht=32±3%、TP=6.0±0.5g/dL(牛血)
- 循環開始24時間後のサイトカイン吸着能、初期濃度10,000pg/mL, QB=100±4mL/min、QF=0mL/min、 37±1℃、TP=6.0±0.5g/dL(牛血漿1L)

電子添文
ヘモフィール®SNV

| 販売名 | ヘモフィール®SNV |
|---|---|
| 一般的名称 | 持続緩徐式血液濾過器 |
| 承認番号 | 23000BZX00297000 |
| クラス分類 | 高度管理医療機器(クラスⅢ) |
| 特定保険医療材料 | 保険償還 II 040 人工腎臓用特定保険医療材料(回路を含む。) (4)持続緩徐式血液濾過器 ① 標準型 ア 一般用 SNV-0.8、SNV-1.0、SNV-1.3 |
| 製造販売元 | 東レ株式会社 |
| 販売元 | 東レ・メディカル株式会社 |
型番・仕様等
- 性能はIn vitro値であり、臨床では使用条件の違いにより異なります。
- ご使用に際しては製品の注意事項等情報をご参照下さい。
- 測定方法:JIS T 3250:2013 限外濾過率による
測定条件:牛血(Ht=32±3%、TP=6.0±0.5g/dL)、37±1℃、QB=100±4mL/min、TMP=6.7kPa

電子添文
保険適用条件
持続緩徐式血液濾過の保険適用条件(対象患者)は、以下の通りです。
J038-2 持続緩徐式血液濾過
使用した特定保険医療材料については、持続緩徐式血液濾過器として算定する。
-
持続緩徐式血液濾過は、次のアからケまでに掲げるいずれかの状態の患者に算定できる。
ただし、キ及びクの場合にあっては一連につき概ね8回を限度とし、ケの場合にあっては一連につき月10 回を限度として3月間に限って算定する。- ア末期腎不全の患者
- イ急性腎障害と診断された高度代謝性アシドーシスの患者
- ウ薬物中毒の患者
- エ急性腎障害と診断された尿毒症の患者
- オ急性腎障害と診断された電解質異常の患者
- カ急性腎障害と診断された体液過剰状態の患者
- キ急性膵炎診療ガイドライン2015において、持続緩徐式血液濾過の実施が推奨される重症急性膵炎の患者
- ク重症敗血症の患者
- ケ劇症肝炎又は術後肝不全(劇症肝炎又は術後肝不全と同程度の重症度を呈する急性肝不全を含む。)の患者
(2)のアからカまでのいずれかに該当する場合は、診療報酬明細書の摘要欄に該当項目を記載すること。
(2)のキからケまでのいずれかに該当する場合は、診療報酬明細書の摘要欄に(2)のキからケまでのそれぞれについて、要件を満たす医学的根拠について記載すること。
人工腎臓、腹膜灌流又は持続緩徐式血液濾過を同一日に実施した場合は、主たるものの所定点数のみにより算定する。
「注1」の加算を算定する場合は、区分番号「A000」初診料の注9及び区分番号「A001」再診料の注7に掲げる夜間・早朝等加算は算定しない。
持続緩徐式血液濾過を夜間に開始した場合とは、午後6時以降に開始した場合をいい、終了した時間が午前0時以降であっても、1日として算定する。ただし、夜間に持続緩徐式血液濾過を開始し、12時間以上継続して行った場合は、2日として算定する。
-
妊娠中の患者以外の患者に対し、持続緩徐式血液濾過と人工腎臓を併せて1月に15回以上実施した場合(持続緩徐式血液濾過のみを15 回以上実施した場合を含む。)は、15回目以降の持続緩徐式血液濾過又は人工腎臓は算定できない。ただし、薬剤料又は特定保険医療材料料は別に算定できる。
(令和6年3月5日保医発0305第4号別添1)
※ヘモフィール®は重症敗血症に対しては適用がありません。
施行方法
- 中空糸の内側、外側をそれぞれ生理食塩液等の電解質輸液で洗浄します。
- ブラッドアクセス部位は、大腿動静脈、鎖骨下動静脈等の通常の体外循環療法で用いる血管とします。
- 回路内のプライミング液が全て入れ替わるまでは、血液流量20~30mL/minで、続いて濾過器、回路内に血液を充填させた後は、血液流量50~60mL/minに上げます。少なくとも開始後5~10分間は血液灌流のみ行い、血液灌流が安定した後、血液濾過を開始します。
- 濾過器内での血液凝固を防止する目的で抗凝固薬を持続注入で投与します。
- 治療終了後は、生理食塩液または5%ブドウ糖液100~200mLを患者の状態をみながら低流量(約50mL/min)で流して、濾過器内および血液回路内の血液を患者に戻します。
- 詳しくは電子添文を参照下さい。
使用上の注意
【警告】
- 治療中は、患者について常に十分な観察を行うこと。[患者によっては治療中に血圧低下等の重篤なショック症状が現れる事がある。また長時間抗凝固剤を使用して治療を行うことから出血または凝固傾向が生じることがある。]
【禁忌・禁止】
- 再使用禁止。
【使用上の注意】
〈使用注意(次の患者には慎重に適用すること)〉
-
特に次の患者には低血液流量、低除水流量で開始し、患者の状態に十分注意し、異常が認められた場合には使用を中止する等、適切な処置を行うこと。[治療時に血圧低下、不均衡症候群などが起こることがある。]
-
①
低体重・低栄養・導入期の患者、循環器合併症患者といった急激な血液濃度の変化や急激な除水に耐えられない患者
-
②
本製品を使用する前に血液透析を行っていた患者
-
③
低血圧及びショック状態といった循環動態が不安定な患者
-
④
本品を使用する前により小膜面積のヘモフィルタ、膜材質又は性能の異なるヘモフィルタを使用していた患者
-
⑤
短時間に急激な除水を必要とする患者
-
-
次の患者については治療中、常に十分な観察を行い、異常が認められた場合には使用を中止するなど適切な処置を行うこと。[血圧低下等の症状が起こることがある。]
-
①
本品を初めて使用する患者
-
②
アレルギー反応、過敏症の既往症のある患者
-
③
これまでに血液浄化療法により血圧低下を経験したことのある患者
-
④
炎症反応、アレルギー反応、過敏症、又は感染症等により免疫機能が亢進している患者
-
⑤
降圧剤(アンジオテンシン変換酵素阻害剤、Ca拮抗剤等)を使用している患者
-
<重要な基本的注意>
- 治療中の異常な症状、症候の発生を避けるため、血液流量、濾過流量、補充液流量及び除水速度を患者の状態に合わせて設定すること。
- 補充液量の制御・監視が可能な装置を用い、除水管理には制御装置を使用すること。治療中の除水過多や水分過剰による異常な症状の発生を避けるため、治療中に補充液量、濾液量及び除水量の正確な監視をすること。
- 本品は66kPa(500mmHg)以下の圧力で使用し、血液濾過中は血液回路内圧を監視すること。
- 包装は使用直前に開封し、洗浄・プライミング終了後は速やかに治療を開始すること。[開封後速やかに使用しないと感染に至るおそれがある。]
- 本品及び血液回路内に空気を混入させないように十分注意すること。[空気が混入していると血液凝固等の原因になることがある。]
- 本品の使用中は、定期的に接続部の緩み、気泡の発生・混入、リーク、血液凝固、溶血、破損、血液漏れ、濾液漏れ、空気混入および詰まり等を確認すること。また、異常が認められた場合には、一時治療を中止するなど適切な処置を行うこと。
- 本体容器や中空糸など製品が破損するリスクがあるので、本製品の運搬、操作時には振動や衝撃を避けること。
- 本品を鉗子等で叩かないこと。[本体容器、ヘッダー、中空糸が破損するおそれがある。]
- 血液ポート及び濾液ポートの栓がはずれていたり、液漏れをしている場合は使用しないこと。
- 本品にアルコール等の有機溶剤製品を含む薬剤が付着しないように十分注意すること。[変形や亀裂が発生する可能性がある。]
- 本品が破損する恐れがあるので、充填液の凍結は避けること。万一、凍結した場合や凍結が危惧される場合は、使用しないこと。
- 返血を行うときには生理食塩液あるいは電解質輸液による置換返血法を用いること。
〈相互作用(他の医薬品・医療機器等との併用に関すること)〉
-
併用注意(併用に注意すること)
- 海外においてある種の合成膜を用いた血液透析で、アンジオテンシン変換酵素阻害剤を服用中の患者が、透析中にアナフィラキシーを発現した報告がある。1)
〈その他の注意〉
- 本品を使用する装置の操作方法については、装置の電子添文及び取扱説明書に従うこと。
- 本品は長時間使用により、圧力が上昇し循環自体が困難になる可能性があるため、24時間を使用の目安として、交換を検討すること。